ミチーガの最新の話題
- 2024年6月 6歳以上の小児に適応拡大されました。
- 2024年6月 結節性痒疹に適応追加されました。
- 2023年6月 自己注射ができるようになりました。
ミチーガとは?
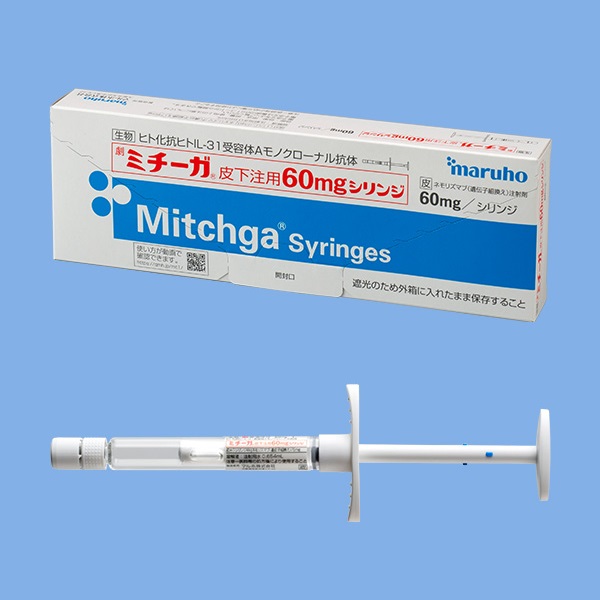
ミチーガ皮下注用60mgシリンジ(有効成分:ネモリズマブ)は、アトピー性皮膚炎の「かゆみ」を誘発するサイトカインであるIL-31をターゲットとした日本初、世界初のヒト化抗ヒトIL-31受容体Aモノクローナル抗体である生物学的製剤です。中外製薬株式会社により創製され、マルホ株式会社が国内第三相臨床試験を実施し、2022年3月に製造販売承認を取得し8月8日に発売されました。
2024年6月11日には小児(6歳以上13歳未満)のアトピー性皮膚炎と、成人及び13歳以上の結節性痒疹で使用可能なミチーガ30㎎バイアルが発売されました。
» 痒疹の詳細はこちら
名称の由来は、mitigate(軽減する)とitch(痒み)を組み合わせてMitigate the Itch(かゆみを和らげる)の意味で、アトピー性皮膚炎患者さんを最も苦しませるかゆみから解放し、QOLの向上した快適な日常を過ごしてほしいという思いが込められて命名されました。
ターゲットはかゆみ
アトピー性皮膚炎は、増悪や寛解を繰り返す、かゆみのある湿疹を主病変とする慢性の皮膚疾患です。かゆみに伴う掻破は、皮膚症状を悪化させ、さらに痒みが増強するという悪循環(Itch-scratchサイクル)を繰り返し、仕事や学業における集中力の低下や睡眠障害などを引き起こし患者さんのQOLを低下させます。
アトピー性皮膚炎のかゆみの原因物質としてヒスタミンがよく知られていますが、抗ヒスタミン薬では完全に抑えられないとされており、アトピー性皮膚炎のかゆみにはIL-31が中心的な役割を果たすと考えられています。ミチーガはIL-31受容体をターゲットとする薬剤であり、既存治療で効果が不十分なアトピー性皮膚炎のかゆみ抑制効果が期待できます。
ミチーガの特徴
ミチーガ(ネモリズマブ)は、アトピー性皮膚炎のかゆみを誘発するサイトカインであるIL-31に着目したお薬です。IL-31は、主にTh2細胞から産生されるサイトカインで、末梢神経に発現するIL-31RA(IL-31受容体)に作用することでかゆみを誘発します。ミチーガはこのIL-31RAに結合することにより、IL-31の結合を阻害し、それに続く細胞内への働きや伝達を阻害することでアトピー性皮膚炎のかゆみを抑制します。
また、IL-31RAは末梢神経のほか、好酸球、好塩基球、肥満細胞などの免疫細胞や角化細胞にも発現していることから、IL-31はかゆみだけでなく、炎症や皮膚のバリア機能低下にも関与していると考えられています。
ミチーガの対象患者さんについて
アトピー性皮膚炎
従来の治療(ステロイド外用剤や抗ヒスタミン剤等による治療)を一定期間続けても十分な効果が得られない場合に投与対象となります。かゆみや皮疹の重症度を確認する必要がありますのでまずはご相談ください。
成人及び13歳以上の小児
ミチーガ60㎎シリンジを使用いたします。
6歳以上13歳未満の小児
ミチーガ30㎎バイアルを使用いたします。
結節性痒疹
従来の治療(ステロイド外用剤や抗ヒスタミン剤等による治療)を一定期間続けても十分な効果が得られない場合に投与対象となります。
成人及び13歳以上の小児
ミチーガ30㎎バイアルを使用いたします。
ミチーガの投与方法と投与スケジュール
アトピー性皮膚炎
成人及び13歳以上の小児
ネモリズマブとして1回60mgを4週間の間隔で皮下投与します。自己注射も出来、室温保存が可能です。
6歳以上13歳未満の小児
ネモリズマブとして1回30㎎を4週間の間隔で皮下投与します。自己注射は出来ませんので、クリニックにて投与します。
結節性痒疹
成人及び13歳以上の小児
ネモリズマブとして初回60㎎を皮下投与し、以降1回30㎎を4週間の間隔で皮下投与します。自己注射は出来ませんので、クリニックにて投与します。
ミチーガの使用上の注意
主な副作用は、アトピー性皮膚炎、皮膚感染症(ヘルペス感染症、蜂巣炎、膿痂疹、二次感染)、上気道炎です。
臨床試験においては皮膚症状の悪化を理由に脱落した患者さんは多くありませんが、原則として、ミチーガ投与開始後も、外用療法(ステロイド薬やプロトピック軟膏、保湿剤など)を併用しながら治療いただきます。
ミチーガの患者負担・薬価について
ミチーガ皮下注用60mgシリンジは1本116,426円で、3割負担の患者さまですと34,928円(薬剤費のみ)となります。
ミチーガ皮下注用30㎎バイアルは1本67,112円で、3割負担の患者さまですと20,134円(薬剤費のみ)となります。
よくあるご質問
- いつからアトピー性皮膚炎のかゆみに効果がありますか?
-
成人及び13歳以上の小児では投与翌日よりプラセボとの有意な改善が認められております。6歳以上13歳未満の小児では開始3日後よりプラセボとの有意な改善が認められております。
患者さまによって異なりますが、通常はミチーガによる治療開始から 16週頃までには効果が現れます。
- いつから結節性痒疹のかゆみに効果がありますか?
-
臨床試験においては投与翌日よりプラセボとの有意な改善が認められております。患者さまによって異なりますが、通常はミチーガによる治療開始から 16週頃までには効果が現れます。
- 自己注射はできますか?
-
ミチーガ60㎎シリンジは2023年6月1日より自己注射が可能になりました。
- 小児への投与はできますか?
-
アトピー性皮膚炎の場合、6歳以上の小児の患者さまに投与可能です。
- 長期投与のデータはありますか?
-
ミチーガの国内における最長投与期間は、国内第Ⅲ相試験の68週です。
- かゆみがおさまれば、ミチーガによる治療を中止してもよいですか?
-
アトピー性皮膚炎は良くなったり悪くなったりを繰り返す疾患です。かゆみがいったんおさまったとしても、治療を中止すると悪化することがあります。経過を見てご相談しながらご判断いたします。
記事制作者
小西真絢(巣鴨千石皮ふ科)
「巣鴨千石皮ふ科」院長。日本皮膚科学会認定専門医。2017年、生まれ育った千石にて 「巣鴨千石皮ふ科」 を開院。
2児の母でもあり、「お肌のトラブルは何でも相談できるホームドクター」を目指しています。